ru
Воробьев Н.А.1,2,3, Михайлов А.В.1, Смирнова Е.В.1,3, Гуцало Ю.В.1, Мартынова Н.И.1
ООО “ЛДЦ МИБС”1, Санкт-Петербург
Санкт-Петербургский Государственный Университет2, Санкт-Петербург
ГБОУ ВПО СЗГМУ им. И.И. Мечникова3, Санкт-Петербург
Воробьев Н.А. к.м.н.
Смирнова Е.В. к.м.н.
Резюме.
Протонная терапия - это новый способ лечения злокачественных опухолей, который может обладать определенными преимуществами перед стандартной фотонной лучевой терапией. Это связано с возможностью создания максимальной дозы излучения в зоне мишени без превышения толерантных доз для нормальных тканей, даже если мишень вплотную прилежит к критическим структурам организма.
В настоящее время идет активное накопление опыта клинического применения протонной терапии. Представленные в статье исследования свидетельствуют о потенциальном преимуществе протонной терапии при лечении опухолей ЦНС, хордом и хондросарком основания черепа и скелета, опухолей головы и шеи, злокачественных опухолей у детей. Активно изучается роль протонов при раке прямой кишки, желудка, предстательной железы, поджелудочной железы. Полученные результаты должны помочь определить группы пациентов, для которых протонная терапия будет иметь решающее значение в улучшении контроля над заболеванием, повышении общей выживаемости и сохранении качества жизни.
Ключевые слова: протонная терапия, хордома, хондросаркома, злокачественные опухоли у детей, радиоиндуцированные опухоли.
Рентгеновское излучение в терапии онкологических заболеваний применяется более 100 лет. На протяжении всего периода существования радиационная онкология постоянно совершенствуется: место гамма-аппаратов заняли высокоэнергетические линейные ускорители, многолепестковые коллиматоры дают возможность создавать поля сложной формы. Методика модулированной по интенсивности лучевой терапии (IMRT) позволяет существенно снизить лучевую нагрузку на здоровые ткани. Интеграция с компьютерной и магнитно-резонансной томографией помогает улучшить визуализацию, определение объемов и зон облучения. Синхронизация облучения с дыханием пациента позволяет компенсировать смещения мишени и органов риска, тем самым повышая эффективность и безопасность лечения.
Противоопухолевый эффект лучевой терапии в большей степени определяется дозой ионизирующего излучения. В тоже время безопасность лечения напрямую зависит от того, насколько удалось снизить лучевую нагрузку на здоровые ткани. Несмотря на технический прогресс, в некоторых случаях методика фотонной терапии не позволяет подвести необходимую тумороцидную дозу таким образом, чтобы избежать тяжелых лучевых повреждений.
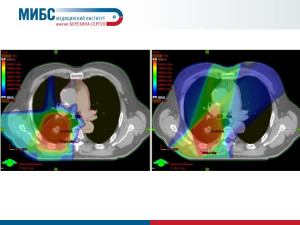
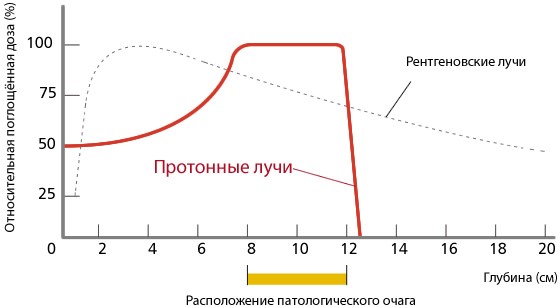
В отличии от других излучений, глубинное распределение дозы для протонов имеет зону медленного подъема с увеличением глубины проникновения, называемую “плато”, за которым следует дозовый максимум, называемый “пиком Брэгга”. Амплитуда этого пика в три-четыре раза превышает дозу на поверхности среды. За пиком Брэгга доза очень быстро падает практически до нуля. Протонная терапия является в настоящее время наиболее мощным средством для получения высокой конформности дозных распределений. На рисунке 1 показаны глубинные распределения доз для ионизирующих излучений. Пониженная величина дозы в области плато по сравнению с дозой в максимуме и быстрый спад дозы за пиком Брэгга создают принципиально новые возможности для формирования “идеальных”распределений дозы. Такая особенность протонной терапии позволяет значительно уменьшить лучевую нагрузку на нормальные ткани по сравнению с традиционными методами лучевой терапии пучками фотонов и электронов. В результате создаются условия для безопасного повышения дозы в объеме мишени (без превышения толерантных доз для нормальных тканей), даже если мишень вплотную прилежит к критическим структурам организма. Более высокая доза приводит, соответственно, к повышению вероятности гибели раковых клеток [1].
Несмотря на очевидные преимущества протонной терапии, клиническая значимость и экономическая эффективность данной методики по-прежнему активно изучаются. С каждым годом проводится все больше исследований по сравнительной оценке протонной и фотонной терапии у пациентов со злокачественными опухолями различных локализаций.
Опухоли центральной нервной системы
У пациентов с опухолями центральной нервной системы (ЦНС) лучевая терапия может применяться на всех этапах лечения – в качестве самостоятельной методики, в послеоперационном периоде, в комбинации с химиотерапией, с радикальной и паллиативной целью. Особенности расположения опухоли существенно ограничивают возможности фотонной лучевой терапии. Доза, необходимая для достижения стойкого контроля над опухолью, зачастую превышает значения, допустимые для органов риска. В подобной ситуации радиотерапевту приходится принимать сложные клинические решения, делая выбор между подведением высокой дозы, способной обеспечить противоопухолевый эффект, и риском повреждения жизненно важных структур. Даже в том случае, если удастся избежать летальных лучевых повреждений, существует высокий риск развития тяжелых нейрокогнитивных расстройств, которые могут быть временными у взрослых, но у детей часто носят необратимый характер. В подобных случаях любые методики, повышающие конформность облучения и позволяющие снизить нагрузку на органы риска (IMRT, протонная терапия), являются предпочтительными. Исследования по сравнению протонной и фотонной лучевой терапии у пациентов с опухолями ЦНС показывают, что применение пучка протонов позволяет значительно снизить нагрузку на здоровые ткани [2].
Хордома, хондросаркома
Заболеваниями, при которых протонная терапия применяется наиболее широко, являются хордомы и хондросаркомы основания черепа. В редких случаях эти опухоли могут быть удалены хирургически. Применение лучевой терапии также ограничено из-за расположения опухоли в непосредственной близости от жизненно важных структур – ствола головного мозга, черепных нервов, спинного мозга. Конформная лучевая терапия в дозах 50-60 Гр не обеспечивает требуемого противоопухолевого эффекта, демонстрируя неудовлетворительные показатели безрецидивной выживаемости (5-летняя безрецидивная выживаемость <25%) [3,4]. Более высокие дозы могут привести к необратимым повреждениям структур головного мозга и летальному исходу. В тоже время, использование протонного пучка позволяет подводить дозы до 72 Гр и более, при этом демонстрируя низкие показатели токсичности [5]. Использование высоких доз способствует значительному повышению безрецидивной выживаемости. Так, в исследованиях, проводимых в клинике Paul Scherrer Institute с применением методики модулированной по интенсивности протонной терапии (IMPT), медиана дозы составила 73,5 Гр при хордоме и 68,4 Гр при хондросаркоме. 5-летняя безрецидивная выживаемость составила 81% и 94% для хордом и хондросарком соответственно. Токсичность 3-4 степени на протяжении 5 лет не превысила 6% [6,7]. Обзор исследований, посвященных применению протонной терапии при хордомах и хондросаркомах, представлен в таблице 1.
Таблица 1. Обзор исследований, посвященных применению протонной терапии при хордомах и хондросаркомах.
| Исследование | N | Патология | Вид лечения | Результат | Токсичность | Заключение |
|---|---|---|---|---|---|---|
|
Rombi и соавт., 2013 [7] |
26 |
Хордомы и хондросаркомы основания черепа |
Хирургия, протонная терапия. Средняя доза 74 Гр для хордомы, 66 Гр для хондросаркомы |
5-летний ЛК 81% для хордомы, 80% для хондросаркомы. 5-летняя ОВ 89% и 85% |
Токсичности IV-V ст. не отмечено |
Высокие показатели ЛК при приемлемой поздней токсичности |
|
McDonald и соавт., 2013 [8] |
16 |
Хордомы основания черепа и позвоночника после хирургического и лучевого лечения |
Повторное облучение протонами, 71,2-79,2 Гр |
2-хлетний ЛК 85% 2-хлетняя ОВ 80% |
Некроз височной доли – 3 пациента. Ишемический инсульт – 1 пациент. |
Повторное облучение протонами возможно рассматривать в качестве метода лечения у пациентов с рецидивами хордом |
|
Ares и соавт., 2009 [6] |
64 |
Хордомы и хондросаркомы основания черепа |
Хирургия, протонная терапия. Средняя доза 68,4 Гр |
5-летний ЛК 81% для хордомы, 94% для хондросаркомы, 5-летняя БРВ 81% и 100%; 5-летняя ОВ 62% и 91% соответственно |
Повреждения зрительного нерва III-IV ст. у 2 пациентов. При 5-летнем наблюдении токсичность IV-V ст. отсутствует у 95% пациентов |
Протонная терапия безопасна и достаточно эффективна |
|
Rutz и соавт., 2008 [9] |
10 |
Хордомы и хондросаркомы основания черепа и позвоночника |
Хирургия, протонная терапия. Средняя доза 66-74 Гр ± химиотерапия |
3-летний ЛК, БРВ и ОВ 100% |
Поздняя токсичность у 3-х пациентов (алопеция, повреждение гипофиза, снижение слуха) |
Модулированная по интенсивности протонная терапия позволяет подводить более высокие дозы |
|
Noel и соавт., 2005 [10] |
100 |
Хордомы основания черепа и позвоночника |
Хирургия, комбинированное облучение протоны+фотоны. Средняя доза 67 Гр |
2-х летний ЛК 86%, 4-х летний ЛК 54%. 2-х летняя ОВ 94%, 5-летняя ОВ 81% |
Поздние осложнения у 42 пациентов (потеря зрения, снижение слуха, повреждение гипофиза) |
Гомогенное распределение дозы в мишени является важным прогностическим фактором |
|
Munzenrider и соавт., 1999 [11] |
519 |
Хордома и хондросаркома основания черепа |
Хирургия, комбинированное облучение протоны+фотоны. Средняя доза 66-83 Гр |
5-летняя БРВ 73% для хордом, 98% для хондросарком. 5-летняя ОВ 80% и 91% соответственно |
3 пациента погибли вследствие повреждения ствола мозга. Также отмечалась потеря слуха, гормональная недостаточность |
Протонная терапия в послеоперационном периоде является методом выбора при хордоме и хондросаркоме основания черепа |
ОВ – общая выживаемость, ЛК – локальный контроль, БРВ – безрецидивная выживаемость
Поскольку для хордом и хондросарком свойственна высокая частота рецидивирования, пациенты часто нуждаются в проведении повторных курсов облучения. В 2013 году McDonald и соавторы опубликовали результаты проведения повторного курса протонной терапии у 16 пациентов с рецидивом хордомы. У 8 пациентов перед повторным облучением было выполнено частичное удаление опухоли. Двухлетняя безрецидивная выживаемость составила 85%, двухлетняя общая выживаемость – 80%. Нежелательные явления 4 степени были отмечены у 1 пациента, токсичности 5 степени отмечено не было. Полученные результаты свидетельствуют о том, что протонная терапия может эффективно применяться при необходимости проведения повторных курсов облучения по поводу рецидивов, демонстрируя высокие показатели локального контроля и выживаемости в тех ситуациях, когда выбор лечебных методик ограничен [8].
Рак легкого
Стандартом лечения неоперабельных форм местнораспространенного немелкоклеточного рака легкого (НМРЛ) является проведение комбинированной химиолучевой терапии. При этом показатели выживаемости нельзя назвать удовлетворительными, в то время как большинство пациентов страдают от выраженной токсичности, связанной с лечением. При проведении лучевой терапии в дозах 60-64 Гр в комбинации с химиотерапией 5-летняя выживаемость не превышает 18%, частота рецидивов достигает 80%. Более чем у 50% пациентов отмечаются серьезные, жизнеугрожающие токсические реакции, такие как пневмонит и эзофагит [12,13]. Исследования по изучению эскалации дозы фотонов до 74 Гр показали, что наряду со снижением риска рецидива, существенно возрастает частота летальных осложнений [14]. Как следствие, смертность от лучевых реакций превышает возможные положительные эффекты при использовании высоких доз излучения [15,16]. Эти результаты свидетельствуют о том, что дальнейшее повышение дозы при использовании фотонов у пациентов с местнораспространенным НМРЛ, по всей видимости, невозможно.
В тоже время, в исследовании, проведенном в клинике MD Anderson Cancer Center, было продемонстрировано, что применение протонной терапии в дозе 74 Гр позволяет повысить медиану выживаемости (29,4 месяца), снизив частоту рецидивов до 20%, а также значительно снижает частоту и выраженность лучевых реакций (дерматит 11%, эзофагит 11%, пневмонит 2%) [17].
Полученные результаты свидетельствуют в пользу возможной эскалации дозы при помощи протонной терапии с целью увеличения выживаемости, снижения частоты рецидивов, снижения токсичности и возможной интенсификации химиотерапии. В клинике MD Anderson Cancer Center в настоящее время идет набор пациентов в исследование 3 фазы по сравнительной оценке фотонной и протонной лучевой терапии у пациентов с местнораспространенным НМРЛ.
Рак предстательной железы
Преимущества применения протонной терапии в лечении рака предстательной железы (РПЖ) на сегодняшний день не очевидны. Конкуренция с другими лечебными методиками (простатэктомия, брахитерапия, 3D-конформная лучевая терапия с IMRT, высокодозная стереотаксическая лучевая терапия) и высокая стоимость пока не позволяют назвать протонную терапию методом выбора при РПЖ.
Результаты клинических исследований показывают, что с увеличением дозы излучения снижается риск развития рецидива РПЖ. В тоже время снижение лучевой нагрузки на стенку мочевого пузыря и прямой кишки значительно снижает частоту и выраженность осложнений. Предполагается, что современные технологии, позволяющие обеспечить высокую конформность, такие как IMRT и протонная терапия, позволят повысить дозу излучения для повышения эффективности терапии без существенного ущерба для здоровых тканей.
Сегодня, благодаря методике IMRT, при помощи фотонной терапии возможно подводить до 80 Гр к предстательной железе без значимого повышения токсичности. Так в исследовании, проведенном в клинике Memorial Sloan-Kettering Cancer Center, 561 пациенту было выполнено облучение предстательной железы в дозе 81 Гр. При этом токсичность второй и более степени со стороны прямой кишки составила лишь 1,6%, со стороны мочевого пузыря – 12% [18]. В тоже время известно, что доза свыше 82 Гр существенно повышает риск кровотечений из прямой кишки, что является существенным лимитирующим фактором [19]. Пока нет ответа на вопрос, возможно ли при помощи протонной терапии существенно повысить дозу излучения, оставаясь при этом в пределах толерантных значений для здоровых тканей.
Одним из возможных путей для обоснованного и более широкого применения протонной терапии при РПЖ, позволяющим не только повысить эффективность и безопасность облучения, но и снизить стоимость лечения, является сокращение количества фракций и укорочение курса лучевой терапии с 7 – 9 недель до одной [20]. Для определения места протонов в лечении РПЖ необходимо проведение проспективных рандомизированных исследований.
Опухоли головы и шеи
В большом количестве работ по сравнительной оценке планов облучения и дозного распределения при использовании протонной и фотонной терапии у пациентов с опухолями головы и шеи отмечено существенное снижение лучевой нагрузки на органы риска в случае применения протонов [21,22,23,24,25,26,27].
Предпочтительной тактикой терапии опухолей полости носа и околоносовых пазух является комбинация хирургического лечения с последующим курсом лучевой терапии. Однако эффективность подобного лечения не может считаться удовлетворительной. Безрецидивная 5-летняя выживаемость при стадиях T1-T3 не превышает 82%, при стадии T4 – 50% [28]. В тоже время частота и тяжесть осложнений, связанных с лечением, заставляет снижать дозу, проводить незапланированные перерывы в облучении и заканчивать курс ранее запланированного срока. Подведение тумороцидных доз к опухолям, расположенным в области основания черепа, затруднено, а в некоторых случаях невозможно по причине близкого расположения ствола головного мозга. Применение фотонной 3D-конформной лучевой терапии при опухолях околоносовых пазух приводит к слепоте вследствие ретинопатии или нейропатии зрительного нерва у 24-40% пациентов [29,30,31]. Работы по сравнительной оценке дозного распределения показали явное преимущество протонной терапии по сравнению с 3D-конформной лучевой терапией и IMRT у пациентов с опухолями полости носа и околоносовых пазух [32]. В исследование Okano и соавт. было включено 13 пациентов с синоназальной карциномой T4b стадии, которым проводилась химиотерапия с последующим курсом протонной лучевой терапии. Полный регресс был отмечен у 85% пациентов, потери зрения или некроза головного мозга не выявлено ни у одного пациента [33]. В другом исследовании оценивались возможности протонной терапии в комбинации с хирургическим и лекарственным лечением у пациентов с опухолевым поражением клиновидных пазух. Показатели двухлетнего локального контроля при дозе 76 Гр составили 86%, 2-летняя безрецидивная выживаемость 31%, 2-летняя общая выживаемость 53%. У 6 пациентов отмечен мукозит 3 степени, офтальмопатии 3-4 степени не выявлено [34].
В терапии опухолей носоглотки и ротоглотки предпочтение отдается химиолучевому лечению. Современная фотонная терапия с применением методики IMRT позволяет снизить частоту таких осложнений, как ксеростомия и дисфагия. Однако исследования по сравнительной оценке дозного распределения показали существенное преимущество протонной терапии, заключающееся в лучшем покрытие мишени предписанной дозой излучения и снижении нагрузки на здоровые ткани [35,36,37,38,39]. Ввиду данного обстоятельства протонная терапия может применяться не только в терапии первичных опухолей носо- и ротоглотки, но и у пациентов с рецидивом после лучевого лечения. В исследовании Lin и соавторов представлен опыт лечения 16 пациентов с рецидивом опухоли носоглотки после курса фотонной лучевой терапии. Облучение протонами проводилось в дозах 60-70 Гр. Показатели двухлетнего локального контроля и безрецидивной выживаемости составили 50% [40]. Из серьезных нежелательных явлений отмечены язва слизистой носоглотки (1 пациент) и остеонекроз (1 пациент). Осложнений со стороны органов центральной нервной системы не отмечено.
Обзор исследований, посвященных применению протонной терапии при опухолях головы и шеи, представлен в таблице 2.
Таблица 2. Обзор исследований, посвященных применению протонной терапии при опухолях головы и шеи
| Исследование | N | Патология | Вид лечения | Результат | Токсичность | Заключение | |
|---|---|---|---|---|---|---|---|
|
Опухоли полости носа и околоносовых пазух |
|||||||
|
Fukumitsu и соавт., 2012 [41] |
17 |
T4 + рецидивные опухоли |
Протонная терапия. Средняя доза 78 Гр, ограничение на хиазму и ствол мозга 50 Гр |
2-хлетний ЛК 35% 5-летний ЛК 17,5% 2-хлетняя ОВ 47,1% 5-летняя ОВ 15,7% |
Токсичность >III ст. у 2-х пациентов (некроз головного мозга, потеря зрения на стороне облучения) |
Протонная терапия позволяет существенно снизить дозу на хиазму и ствол мозга у пациентов с неоперабельными опухолями |
|
|
Okano и соавт., 2012 [33] |
13 |
T4b |
Химиотерапия, протонная терапия ± цисплатин |
Полный регресс 85% |
Потери зрения, некроза мозга не отмечено |
Протонная терапия позволяет проводить химиолучевое лечение при T4b стадии |
|
|
Zenda и соавт., 2011 [42] |
39 |
Нерезектабель-ные опухоли |
Протонная терапия. Средняя доза 65 Гр |
1-летний ЛК 77% 3-хлетняя БРВ 49% 3-хлетняя ОВ 59% |
Ранней токсичности III-V ст. не отмечено. Поздняя токсичность III-V ст. – 12,8% |
Протонная терапия позволяет добиться высоких результатов при нерезектабельных опухолях |
|
|
Resto и соавт., 2008 [43] |
102 |
Местно-распространенная синоназальная карцинома |
Протонная терапия или протоны+фотоны, ± хирургическое лечение. Средняя доза 71,6 Гр |
5-летний ЛК 95% 5-летняя БРВ 90% 5-летняя ОВ 90% |
Н.д. |
Протонная терапия позволяет добиться высоких показателей ЛК. Полное удаление опухоли ассоциируется с высокими показателями БРВ |
|
|
Опухоли носоглотки |
|||||||
|
Lin и соавт., 1999 [40] |
16 |
Рецидивы после лучевой терапии |
Повторное облучение, протонная терапия. Средняя доза 59,4 – 70,2 Гр |
2-х летняя БРВ 50% 2-х летняя ОВ 50% |
Не отмечено тосичности со стороны ЦНС |
Лучшее покрытие мишени способствует увеличению ОВ |
|
|
Опухоли ротоглотки |
|||||||
|
Slater и соавт., 2005 [44] |
29 |
II-IV стадии |
Протонная + фотонная терапия. 75,9 Гр |
5-летний ЛК 84% 5-летняя БРВ 65% |
Поздняя токсичность III ст. у 3-х пациентов |
Протонная терапия в качестве последовательного буста после фотонной терапии позволяет подводить высокие дозы, сохраняя токсичность на приемлемом уровне |
|
ОВ – общая выживаемость, ЛК – локальный контроль, БРВ – безрецидивная выживаемость
Злокачественные опухоли у детей
Согласно данным РОНЦ им. Н.Н. Блохина, онкологическая заболеваемость в России составляет 9,5 – 13 на 100.000 детского населения. Среднее число ежегодно регистрируемых детей со злокачественными опухолями увеличилось за последнее десятилетие на 20% и достигло 6,45 тысяч. В большинстве случаев лучевая терапия является неотъемлемым компонентом, значительно повышая эффективность лечения. В тоже время, облучение способно оказывать пагубное воздействие, замедляя рост и развитие костей, мышц, органов нервной системы. Также повышается риск развития радиоиндуцированных опухолей
По данным литературы, риск развития вторичных радиоиндуцированных опухолей у пациентов, в детстве получавших лучевую терапию по поводу злокачественных новообразований ЦНС, составляет 10,7% [45]. Вторичные опухоли являются второй по частоте причиной смерти у данной группы пациентов [46]. Также они являются основной причиной гибели тех, кто преодолел 10-летний рубеж с момента лечения [47].
Среди вторичных радиоиндуцированных опухолей у пациентов, получавших в детском возрасте лечение по поводу новообразований ЦНС, наиболее часто встречаются глиомы, менингиомы, саркомы, злокачественные опухоли щитовидной железы [48]. Установлено, что радиоиндуцированные глиомы развиваются в среднем спустя 9 лет, а менингиомы спустя 17 лет после лечения.
В немногочисленных клинических исследованиях отмечено, что проведение протонной терапии сопровождается существенно меньшим риском развития вторичных радиоиндуцированных опухолей, нежели при использовании фотонов. В одном из ретроспективных исследований оценивался риск развития вторичных опухолей у взрослых, получавших протонную и фотонную лучевую терапию. В каждую группу было набрано по 558 пациентов. Медиана наблюдения в группе протонной терапии составила 6,7 лет, в группе фотонной терапии – 6 лет. Частота развития вторичных опухолей после облучения протонами была ниже и составила 6,9 случаев на 1000 пациентов против 10,3 в группе фотонной терапии [49].
Применение протонной терапии при краниоспинальном облучении также должно способствовать снижению риска развития радиоиндуцированных опухолей. В исследованиях, основанных на математическом моделировании и данных о биологических эффектах ионизирующего излучения, предиктивный риск развития вторичных опухолей оказался в 4 – 10 раз выше, а предиктивный риск смерти от вторичных опухолей в 2 – 5 раз выше при использовании фотонной лучевой терапии, чем в случае применения протонов [50]. При оценке рисков, связанных с проведением краниоспинального облучения у пациентов с медуллобластомой было установлено, что вероятность развития радиоиндуцированных опухолей при использовании протонной терапии существенно ниже, чем при использовании фотонов и составляет 4% и 30% соответственно (Таб. 3) [51]. Показатели лучевой нагрузки на улитку и сердце при проведении краниоспинального облучения с применением различных методик лучевой терапиипредставлены в таблице 4 [52].
Таблица 3. Вероятность развития радиоиндуцированных опухолей после краниоспинального облучения при медуллобластоме
| Вид лучевой терапии | Риск развития радиоиндуцированных опухолей, % |
|---|---|
|
Фотонная лучевая терапия (IMRT) |
30% |
|
3D-конформная фотонная лучевая терапия |
20% |
|
Протонная терапия |
4% |
Таблица 4. Показатели лучевой нагрузки на улитку и сердце при проведении краниоспинального облучения по поводу медуллобластомы в зависимости от методики лучевой терапии
| Вид лучевой терапии | Доза на 90% объема улитки, % | Доза на 50% объема сердца, % |
|---|---|---|
|
3D-конформная фотонная лучевая терапия |
101,2 |
72,2 |
|
Фотонная лучевая терапия (IMRT) |
33,4 |
29,5 |
|
Протонная терапия |
2,4 |
0,5 |
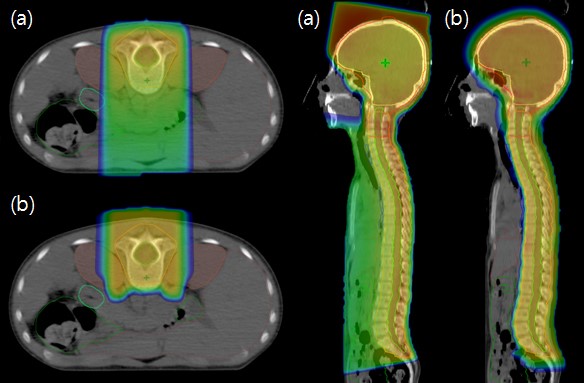
Подобное преимущество протонной терапии является следствием значительного снижения лучевой нагрузки на здоровые ткани (Рис. 2) и наблюдается не только в случае краниоспинального облучения, но и при лечении ретинобластом, сарком костей и мягких тканей, рабдомиосарком и других злокачественных опухолей [53,54]. Снижение риска развития вторичных радиоиндуцированных опухолей является важным фактором, свидетельствующим о необходимости применения протонной терапии у пациентов детского возраста.
В ряде исследований было отмечено, что снижение риска развития постлучевых осложнений при использовании протонной терапии также приводит к значительному снижению финансовой нагрузки на систему здравоохранения за счет уменьшения расходов на лечение осложнений. Значительная экономия средств достигается путем снижения частоты развития таких побочных эффектов как потеря слуха, потеря зрения, кардиотоксичность, развитие радиоиндуцированных опухолей. Экономические расчеты, выполненные в условиях Шведской системы здравоохранения, показали более чем двукратное снижение расходов на лечение постлучевых осложнений в случае применения у детей протонной терапии, в отличии от фотонного облучения (Таб. 5) [55]. Снижение дозы на гипоталамус на 10 Гр при использовании протонов значительно снижает риск развития гормональной недостаточности и, следовательно, позволяет сократить расходы на проведение последующей заместительной гормонотерапии [56].
Таблица 5. Стоимость фотонной и протонной лучевой терапии при медуллобластоме
| Фотонная терапия | Протонная терапия | Различие | |
|---|---|---|---|
|
Лучевая терапия |
5,622$ |
13,552$ |
x2,5 |
|
Лечение осложнений |
44,905$ |
5,613$ |
x8 |
|
Всего |
50,527$ |
19,165$ |
x2,6 |
Помимо перечисленных в данной статье злокачественных опухолей, протонная терапия также может иметь потенциальное преимущество при лечении рака прямой кишки, желудка, поджелудочной железы, опухолей костей и мягких тканей (за счет снижения лучевой нагрузки на кишечник, мочевой пузырь, легкие, спинной мозг). Уменьшение патологического воздействия на костный мозг и снижение гематологической токсичности может способствовать более активному применению химиотерапии конкурентно с протонной лучевой терапией [57].
В настоящее время идет активное накопление опыта клинического применения протонной терапии. Ежегодно стартуют новые проспективные исследования, посвященные изучению роли протонов в лечении онкологических заболеваний. Полученные результаты должны помочь определить группы пациентов, для которых протонная терапия будет иметь решающее значение в улучшении контроля над заболеванием, повышении общей выживаемости и сохранении качества жизни.
Список литературы
- Климанов В. А. // Радиобиологическое и дозиметрическое планирование лучевой и радионуклидной терапии. Часть 2. Лучевая терапия пучками протонов, ионов, нейтронов и пучками с модулированной интенсивностью, стереотаксис, брахитерапия, радионуклидная терапия, оптимизация, гарантия качества. - Учебное пособие. М.: НИЯУ МИФИ. - 2011.
- Suit H, Goldberg S, Niemierko A, et al. Proton beams to replace photon beams in radical dose treatments // Acta Oncol. 2003. Vol. 42. P. 800–808.
- Catton C, O’Sullivan B, Bell R, et al. Chordoma: Long-term followup after radical photon irradiation // Radiother. 1996. Vol. 41. P. 67-72.
- Zorlu F, Gurkaynak M, Yildiz F, et al. Conventional external radiotherapy in the management of clivus chordomas with overt residual disease // Neurol Sci. 2000. Vol. 21. P. 203-207.
- Santoni R, Liebsch N, Finkelstein DM, et al. Temporal lobe (TL) damage following surgery and high-dose photon and proton irradiation in 96 patients affected by chordomas and chondrosarcomas of the base of the skull // Int J Radiat Oncol Biol Phys. 1998. Vol. 41. P. 59–68.
- Ares C, Hug EB, Lomax AJ, et al. Effectiveness and safety of spot scanning proton radiation therapy for chordomas and chondrosarcomas of the skull base: First long-term report // Int J Radiat Oncol Biol Phys. 2009. Vol. 75. P. 1111-1118.
- Rombi B, Ares C, Hug EB, et al. Spot-scanning proton radiation therapy for pediatric chordoma and chondrosarcoma: Clinical outcome of 26 patients treated at Paul Scherrer Institute // Int J Radiat Oncol. 2013. Vol. 86. P. 578-584.
- McDonald MW, Linton OR, Shah MV. Proton therapy for reirradiation of progressive or recurrent chordoma // Int J Radiat Oncol Biol Phys. 2013. Vol. 87. P. 1107-1114.
- Rutz HP, Weber DC, Goitein G, et al. Postoperative spot-scanning proton radiation therapy for chordoma and chondrosarcoma in children and adolescents: Initial experience at Paul Scherrer Institute // Int J Radiat Oncol Biol Phys. 2008. Vol. 71. P. 220-225.
- Noel G, Feuvret L, Calugaru V, et al. Chordomas of the base of the skull and upper cervical spine. One hundred patients irradiated by a 3D conformal technique combining photon and proton beams // Acta Oncol. 2005. Vol. 44. P. 700-708.
- Munzenrider JE, Liebsch NJ. Proton therapy for tumors of the skull base // Strahlenther Onkol. 1999. Vol. 175(Suppl 2). P. 57-63.
- Curran WJ Jr, Paulus R, Langer CJ, et al. Sequential vs. concurrent chemoradiation for stage III non-small cell lung cancer: randomized phase III trial RTOG 9410 // J Natl Cancer Inst. 2011. Vol. 103 (19). P. 1452–1460.
- Zatloukal P, Petruzelka L, Zemanova M, et al. Concurrent versus sequential chemoradiotherapy with cisplatin and vinorelbine in locally advanced non-small cell lung cancer: a randomized study // Lung Cancer. 2004. Vol. 46(1). P. 87–98.
- Schild SE, McGinnis WL, Graham D, et al. Results of a Phase I trial of concurrent chemotherapy and escalating doses of radiation for unresectable non-small-cell lung cancer // Int J Radiat Oncol Biol Phys. 2006. Vol. 65(4). P. 1106–1111.
- Bradley JD, Paulus R, Komaki R, et al. A randomized phase III comparison of standard-dose (60 Gy) versus high-dose (74 Gy) conformal chemoradiotherapy +/? cetuximab for stage IIIA/IIIB nonsmall cell lung cancer: preliminary findings on radiation dose in RTOG 0617 [abstract] // Miami Beach, FL: 53rd Annual Meeting of the American Society for Radiation Oncology. 2011.
- Cox JD: Are the results of RTOG 0617 mysterious? // Int J Radiat Oncol Biol Phys. 2012. Vol. 82(3). P. 1042–1044.
- Sejpal S, Komaki R, Tsao A, et al. Early Findings on Toxicity of Proton Beam Therapy with Concurrent Chemotherapy in Nonsmall Cell Lung Cancer // Cancer. 2011. Vol. 117. P. 3004–3013.
- Zelefsky MJ, Chan H, Hunt M, et al. Long-term outcome of high dose intensity modulated radiation therapy for patients with clinically localized prostate cancer // J Urol. 2006. Vol. 176(4 Pt 1). P. 1415–1419.
- Coen JJ, Bae K, Zietman AL, et al. Acute and late toxicity after dose escalation to 82 GyE using conformal proton radiation for localized prostate cancer: initial report of American College of Radiology Phase II study 03-12 // Int J Radiat Oncol Biol Phys. 2011. Vol. 81. P. 1005–1009.
- King CR, Brooks JD, Gill H, Presti JC Jr: Long-term outcomes from a prospective trial of stereotactic body radiotherapy for low-risk prostate cancer // Int J Radiat Oncol Biol Phys. 2012. Vol. 82(2). P. 877–882.
- Van de Water TA, Lomax AJ, Bijl HP, et al. Potential benefits of scanned intensity-modulated proton therapy versus advanced photon therapy with regard to sparing of the salivary glands in oropharyngeal cancer // Int J Radiat Oncol Biol Phys. 2011. Vol. 79. P. 1216-1224.
- Steneker M, Lomax A, Schneider U. Intensity modulated photon and proton therapy for the treatment of head and neck tumors // Radiother Oncol. 2006. Vol. 80. P. 263-267.
- Miralbell R, Crowell C, Suit HD. Potential improvement of three dimension treatment planning and proton therapy in the outcome of maxillary sinus cancer // Int J Radiat Oncol Biol Phys. 1992. Vol. 22. P. 305-310.
- Miralbell R, Lomax A, Cella L, et al. Potential reduction of the incidence of radiation-induced second cancers by using proton beams in the treatment of pediatric tumors // Int J Radiat Oncol Biol Phys. 2002. Vol. 54. P. 824-829.
- Van de Water TA, Lomax AJ, Bijl HP, et al. Using a reduced spot size for intensity-modulated proton therapy potentially improves salivary gland-sparing in oropharyngeal cancer // Int J Radiat Oncol Biol Phys. 2012. Vol. 82. P. e313-e319.
- Yoon M, Ahn SH, Kim J, et al. Radiation-induced cancers from modern radiotherapy techniques: Intensity-modulated radiotherapy proton therapy // Int J Radiat Oncol Biol Phys. 2010. Vol. 77. P. 1477-1485.
- Weber DC, Chan AW, Lessell S, et al. Visual outcome of accelerated fractionated radiation for advanced sinonasal malignancies employing photons/protons // Radiother Oncol. 2006. Vol. 81. P. 243-249.
- Mendenhall WM, Amdur RJ, Morris CG, et al. Carcinoma of the nasal cavity and paranasal sinuses // Laryngoscope. 2009. Vol. 119. P. 899-906.
- Waldron JN, O’Sullivan B, Warde P, et al. Ethmoid sinus cancer: Twenty-nine cases managed with primary radiation therapy // Int J Radiat Oncol Biol Phys. 1998. Vol. 41. P. 361-369.
- Takeda A, Shigematsu N, Suzuki S, et al. Late retinal complications of radiation therapy for nasal and paranasal malignancies: Relationship between irradiated-dose area and severity // Int J Radiat Oncol Biol Phys. 1999. Vol. 44. P. 599-605.
- Katz TS, Mendenhall WM, Morris CG, et al. Malignant tumors of the nasal cavity and paranasal sinuses // Head Neck. 2002. Vol. 24. P.821-829.
- Mock U, Georg D, Bogner J, et al. Treatment planning comparison of conventional, 3D conformal, and intensity-modulated photon (IMRT) and proton therapy for paranasal sinus carcinoma // Int J Radiat Oncol Biol Phys. 2004. Vol. 58. P. 147-154.
- Okano S, Tahara M, Zenda S, et al. Induction chemotherapy with docetaxel, cisplatin and S-1 followed by proton beam therapy concurrent with cisplatin in patients with T4b nasal and sinonasal malignancies // Jpn J Clin Oncol. 2012. Vol. 42. P. 691-696.
- Truong MT, Kamat UR, Liebsch NJ, et al. Proton radiation therapy for primary sphenoid sinus malignancies: Treatment outcome and prognostic factors // Head Neck. 2009. Vol. 31. P. 1297-1308.
- Van der Laan HP, van de Water TA, van Herpt HE, et al. The potential of intensity-modulated proton radiotherapy to reduce swallowing dysfunction in the treatment of head and neck cancer: A planning comparative study // Acta Oncol. 2013. Vol. 52. P. 561-569.
- Van de Water TA, Lomax AJ, Bijl HP, et al. Potential benefits of scanned intensity-modulated proton therapy versus advanced photon therapy with regard to sparing of the salivary glands in oropharyngeal cancer // Int J Radiat Oncol Biol Phys. 2011. Vol. 79. P. 1216-1224.
- Liu SW, Li J-M, Chang J-Y, et al. A treatment planning comparison between proton beam therapy and intensity-modulated x-ray therapy for recurrent nasopharyngeal carcinoma // J Xray Sci Technol. 2010. Vol. 18. P. 443-450.
- Taheri-Kadkhoda Z, Bjork-Eriksson T, Nill S, et al. Intensity modulated radiotherapy of nasopharyngeal carcinoma: A comparative treatment planning study of photons and protons // Radiat Oncol. 2008. Vol. 3. P. 4.
- Widesott L, Pierelli A, Fiorino C, et al. Intensity-modulated proton therapy versus helical tomotherapy in nasopharynx cancer: Planning comparison and NTCP evaluation // Int J Radiat Oncol Biol Phys. 2008. Vol. 72. P. 589-596.
- Lin R, Slater JD, Yonemoto LT, et al. Nasopharyngeal carcinoma: Repeat treatment with conformal proton therapyddose-volume histogram analysis // Radiology. 1999. Vol. 213. P. 489-494.
- Fukumitsu N, Okumura T, Mizumoto M, et al. Outcome of T4 (International Union Against Cancer Staging System, 7th edition) or recurrent nasal cavity and paranasal sinus carcinoma treated with proton beam // Int J Radiat Oncol Biol Phys. 2012. Vol. 83. P. 704-711.
- Zenda S, Kohno R, Kawashima M, et al. Proton beam therapy for unresectable malignancies of the nasal cavity and paranasal sinuses // Int J Radiat Oncol Biol Phys. 2011. Vol. 81. P. 1473-1478.
- Resto VA, Chan AW, Deschler DG, et al. Extent of surgery in the management of locally advanced sinonasal malignancies // Head Neck. 2008. Vol. 30. P. 222-229.
- Slater JD, Yonemoto LT, Mantik DW, et al. Proton radiation for treatment of cancer of the oropharynx: Early experience at Loma Linda University Medical Center using a concomitant boost technique // Int J Radiat Oncol Biol Phys. 2005. Vol. 62. P. 494-500.
- Armstrong, G. T. Long-term survivors of childhood central nervous system malignancies: the experience of the Childhood Cancer Survivor Study // Eur. J. Paediatr. Neurol. 2010. Vol. 14. P. 298–303.
- Mertens, A. C. et al. Cause-specific late mortality among 5-year survivors of childhood cancer: the Childhood Cancer Survivor Study// J. Natl Cancer Inst. 2008. Vol. 100. P. 1368–1379.
- Morris, E. B. et al. Survival and late mortality in longterm survivors of pediatric CNS tumors // J. Clin. Oncol. 2007. Vol. 25. P. 1532–1538.
- Peterson, K. M., Shao, C., McCarter, et al. An analysis of SEER data of increasing risk of secondary malignant neoplasms among long-term survivors of childhood brain tumors // Pediatr. Blood Cancer. 2006. Vol. 47. P. 83–88.
- Chung, C. S. et al. Incidence of second malignancies among patients treated with proton versus photon radiation // Int. J. Radiat. Oncol. Biol. Phys. 2013. Vol. 87. P. 46–52.
- Zhang, R. et al. A comparative study on the risks of radiogenic second cancers and cardiac mortality in a set of pediatric medulloblastoma patients treated with photon or proton craniospinal irradiation // Radiother. Oncol. 2014. Vol. 113. P. 84–88.
- Mu X, Bjork-Eriksson T, Nill S, et al. Does electron and proton therapy reduce the risk of radiation induced cancer after spinal irradiation for childhood medulloblastoma? a comparative treatment planning study // Acta Oncol. 2005. Vol. 44(6). P. 554–562.
- St Clair WH, Adams JA, Bues M, et al. Advantage of protons compared to conventional X-ray or IMRT in the treatment of a pediatric patient with medulloblastoma // Int J Radiat Oncol Biol Phys. 2004. Vol. 58(3). P. 727–734.
- Lee CT, Bilton SD, Famiglietti RM, et al. Treatment planning with protons for pediatric retinoblastoma, medulloblastoma, and pelvic sarcoma: how do protons compare with other conformal techniques? // Int J Radiat Oncol Biol Phys. 2005. Vol. 63(2). P. 362–372.
